Viskas apie osmį

Osmis - retas metalas, priklauso platinos grupei. Jis buvo atrastas Anglijoje atlikus platinos reakcijos eksperimentus. Osmio pavadinimas pateiktas graikų kalba, o vertimas reiškia „kvapas“. Koks yra šis taurusis metalas? Kokios jo savybės ir kokia jo paskirtis?

Istorija
Šį elementą 1803 metais atsitiktinai atrado anglų chemikai Smithson Tennant ir William H. Wollastan. Atlikus platinos reakcijos į rūgščių (sieros ir azoto) mišinį eksperimentus, susidariusiose nuosėdose atsirado nemalonus aromatas, primenantis chloro ir supuvusių ridikėlių smarvę. Panašius eksperimentus atliko Colle-Descoti, Antoine de Fourcoy ir Vauquelin Prancūzijoje. Atlikę tyrimus jie taip pat aptiko nežinomą medžiagą netirpiose platinos nuosėdose.



Tuomet nežinoma medžiaga buvo pavadinta viščiuku, tačiau britų eksperimentai įrodė, kad tai dvi panašios medžiagos – iridis ir osmis.
Šių cheminių elementų atradimas buvo pristatytas Karališkajai Londono draugijai Tennanto 1804 m. birželio 21 d. Mendelejevo cheminių elementų periodinėje lentelėje metalas yra eilės numeriu 76. Metalas grynu pavidalu neatsiranda grynuolių pavidalu, todėl jo cheminė formulė pateikiama ištirpusioje formoje.


Elementas išgaunamas iš antrinių žaliavų dėl jo atskyrimo nuo iridžio, platinos, platinos-paladžio rūdų arba vario ir nikelio rūdų. Metinė viso elemento produkcija pasaulyje neviršija 1 tonos.


Gimimo vieta
Į didžiausius pasaulio telkinius verta atkreipti dėmesį tokios zonos kaip Uralo kalnai ir Sibiras Rusijoje, šiaurinėje valstijoje Aliaska ir vakarų valstija Kalifornija Amerikoje, Kanada Šiaurės Amerikoje, Kolumbija Pietų Amerikoje ir kai kuriose Pietų Afrikos šalys, Australija, sala Tasmanija... Šiuo metu svarstomas didelis osmio telkinys Bushwell kompleksas Pietų Afrikoje, ten išgaunama didžioji dalis medžiagos. Atsižvelgiant į tai, kad didžiausi metalo telkiniai yra Pietų Afrikoje, pasaulinės šio retųjų žemių metalo kainos yra gana aukštos. Kazachstanas yra laikoma vienintele pagrindine osmio-187 eksportuotoja pasaulyje. Nors Kinija turi platinos rūdos atsargų, joje nėra daug osmio.


Medžiaga laikoma miltelių pavidalu ir, kadangi ji nesitirpsta kristalų pavidalu, dėl jos fizinių savybių antspaudo uždėti negalima. Šio metalo luitų gamybai naudojamas kaitinimas elektronų pluoštu arba lanku iš miltelių, taip pat naudojamas kaitinimas tiglyje.


Savybės
Osmis atrodo kaip sidabriškai melsvas metalas. Tai vienas iš tankiausių elementų, jo tankis 22 600 kilogramų kubiniame metre, tačiau tuo pačiu metu medžiaga yra gana trapi, lengvai lūžta ir trupa. Jis turi didelį savitąjį svorį ir gali blizgėti net esant gana aukštai temperatūrai. Dėl savo parametrų ir reikšmingos lydymosi temperatūros jį sunku apdirbti. Gamtoje jis egzistuoja septynių izotopų pavidalu, iš kurių šeši laikomi stabiliais, tai yra osmis-184, osmis-187, osmis-188, osmis-189, osmis-190 ir osmis-192. Laboratorijoje buvo gauti radioaktyvūs metalų izotopai, kurių masės skaičiai nuo 162 iki 197, kai kurie branduoliniai izomerai taip pat buvo gauti dirbtinai.
Osmis pagal savo savybes neigiamai veikia visus gyvus organizmus.

Beveik visi junginiai su šiuo metalu sukelia vidaus organų pažeidimus, regos ir klausos sutrikimus. Apsinuodijus osmio garais galimi negrįžtami organizmo sutrikimai ir mirtis. Mokslininkai atliko eksperimentus su gyvūnais, kurių rezultatai buvo greitas anemijos vystymasis, normalios plaučių funkcijos stoka. Padaryta išvada, kad tai sparčiai besivystanti edema. Osmio tetroksidas, naudojamas medicinoje, yra labai ėsdinanti medžiaga. Turi bjauriausią kvapą pasaulyje. Apsinuodijus kenčia oda, ji keičia spalvą į žalią arba juodą, dažnai kartu atsiranda opų ir įtrūkimų, kurie užgis labai ilgai.

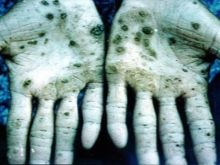

Didžiausia rizika kyla gamybinių patalpų darbuotojams, kurie pagal visus saugos standartus dirba tik su respiratoriais ir specialia apranga. Visos talpyklos, kuriose yra osmio oksido, yra sandariai uždaromos ir laikomos laikantis taisyklių. Norint gauti nevyanskito mineralus, platina paverčiama tirpalu naudojant aqua regia. Tada susidariusios nuosėdos yra veikiamos cinko 8 kartus – toks lydinys gana lengvai paverčiamas miltelių pavidalu, kuris vėliau sulydomas su bario peroksidu. Kitas etapas – gautos masės apdorojimas aqua regia, distiliavimas per osmio tetroksido atskyrimo aparatą.

Veikiant medžiagą šarminiu tirpalu, gaunama druska. Paveikiamas druskos tirpalas hiposulfitas, ko pasekoje amonio chlorido pagalba metalas nusėda jau Fremy druskos pavidalu. Nuosėdos plaunamos, filtruojamos ir kalcinuojamos. Visų šių veiksmų rezultatas yra kempinė osmis. Vėliau jis valomas rūgštimis, redukuojamas elektrinėje krosnyje vandenilio srove ir atšaldomas. Taigi gauti osmio mėginius iki 99,9%.


Cheminis
Šio elemento savybės chemijos požiūriu yra nuostabios. Paprasčiausi iš jų yra šie.
- Osmis visiškai nereaguoja su šarmais ir rūgštimis. Reaguodamas su šarminiais lydalais, susidaro vandenyje tirpūs osmatai. Sąveika su azoto ir druskos rūgščių mišiniu duoda itin lėtą reakciją.
- Labai toksiška, net ir mikroskopinėmis dozėmis. Ypač toksiškas yra osmio oksidas, išsiskiriantis iš platinos.
- Neįmanoma nustatyti metalo virimo temperatūros, nes jis ypač atsparus ugniai.
- Milteliuose esantis metalas lengvai patenka į kaitinimo reakciją su tokiomis medžiagomis: grynu deguonimi, halogenais, sieros arba azoto rūgštimis.
- Įvairiuose junginiuose gaunami oksidų skaičiai nuo -2 iki +8. Labiausiai paplitę yra +2, +3, +4 ir +8.
- Geba sudaryti klasterinius junginius.
- Pagrindiniai mineralai yra susiję su kietaisiais tirpalais ir yra atstovaujami iridžio ir osmio lydiniais - tai sisertskite ir nevyanskite. Be to, siserskite turi kitą pavadinimą - iridious osmium, o nevyanskite - osmosinis iridis.

Fizinis
Tankis osmio yra maždaug 22,61 gramo kubiniame centimetre. Kristalai turi gražų sidabrinį blizgesį, įvairių atspalvių nuo pilkos iki mėlynos. Luituose atsiranda tamsiai mėlyna spalva, milteliuose - violetinė. Visas metalas turi sidabrinį blizgesį. Elemento toksiškumas neleidžia jo naudoti juvelyrikos pramonėje. Pagrindinės fizinės savybės yra šios.
- Šio elemento lydymosi temperatūra yra gana aukšta, lydyti galima aukštesnėje nei 3000 laipsnių Celsijaus temperatūroje.
- Metalas neturi magnetinių savybių.
- Nuostabus tvirtumas. Lydiniai su šio metalo priedu padidina atsparumą dilimui, ilgaamžiškumą, atsparumą korozijai ir atsparumą mechaniniam poveikiui.
- Virimo temperatūra yra 5012 ºC.
- Moho kietumas yra 7.
- Vickers kietumas yra 3-4 GPa.

Programos
Dėl nemažos paties elemento kainos šis metalas retai naudojamas masinėje pramoninėje gamyboje. Osmis daugiausia naudojamas chemijos pramonėje, kur jis naudojamas kaip katalizatorius. Osmio tetroksidas naudojamas kai kuriuose vaistuose. Laboratoriniuose tyrimuose naudojamas gyvų audinių dažymui, užtikrina ląstelių struktūros išsaugojimą.
Aviacijos ir kosmoso pramonėje naudojamas osmis aviacijos ir raketų technologijų įrangos elektroninėje įrangoje, taip pat gamyboje atominiai ginklai. Dėl magnetinių savybių trūkumo, metalas naudojamas gaminant firminius laikrodžius, tokius kaip Rolex. Osmio ir platinos lydinys naudojamas, kai chirurginių implantų kūrimas Ar širdies stimuliatoriai arba plaučių vožtuvai.
Be to, osmis naudojamas mikroskopijoje ir didelio tikslumo instrumentams kurti.



Įdomūs faktai
- Esant maždaug 770 GPa slėgiui osmyje, elektronai sąveikauja vidinėse orbitose, medžiagos struktūra išlieka nepakitusi.
- Osmis uolienose yra pusė procento visos rūdos telkinių masės.
- Dėl didelio tankio metalo išvaizda ir tikrasis svoris labai skiriasi. Taigi, 0,5 litro plastikinis butelis, užpildytas šiais metaliniais milteliais, bus sunkesnis nei 10 litrų kibiras, pripildytas vandens.
- Šis metalas yra daugiausiai penketuke brangus.
- Trigubos osmio uncijos kaina yra komercinė paslaptis, atviruose šaltiniuose galite rasti apytikslę 1 gramo medžiagos kainą.
- Dėl osmio atsparumo ugniai pažymėta elektros lempos istorijoje. Mokslininkas K. Aueris von Welsbachas iš Vokietijos pateikė pasiūlymą pakeisti anglies siūlą elektros lemputėje osmio siūlu. Paaiškėjo, kad lemputės sunaudoja 3 kartus mažiau energijos, o apšvietimas žymiai pagerėjo. Tiesa, netrukus jį pakeitė įprastesnis tantalas, kuris, savo ruožtu, buvo pakeistas volframu.
- Panaši situacija atsitiko ir su retuoju metalu amoniako gamyboje. Šiuo metu naudojamas amoniako sintezės metodas, kurį 1908 metais sukūrė chemikas iš Vokietijos Fritzas Haberis, neįmanomas be katalizatorių.Iš pradžių tuo metu naudoti katalizatoriai rodė savo savybes tik esant reikšmingoms temperatūros sąlygoms ir nepasižymėjo dideliu efektyvumu, todėl pakaitalo paieška buvo labai skubi. Karlsrūhės aukštosios technikos mokyklos laboratorijos mokslininkai pasiūlė kaip katalizinį elementą naudoti smulkiai išpurkštą osmį. Bandymų rezultatai patvirtino, kad ši idėja yra verta, katalizinė temperatūra nukrito daugiau nei 100 ºC, o amoniako išsiskyrimas žymiai padidėjo. Tiesa, ateityje jie atsisakė osmio, bet jis padėjo išspręsti tokią svarbią problemą.

Žaidžia osmis ir kiti reti bei unikalūs metalai vaidina svarbų vaidmenį įvairiose pramonės šakose... Net nepaisant viso savo toksiškumo, jis gelbsti gyvybes ir sveikatą.
Norėdami gauti daugiau informacijos apie osmį, žiūrėkite šį vaizdo įrašą.








